Patente da Semaglutida expira no Brasil nesta sexta-feira, abrindo portas para versões genéricas e mais acessíveis de medicamentos populares.
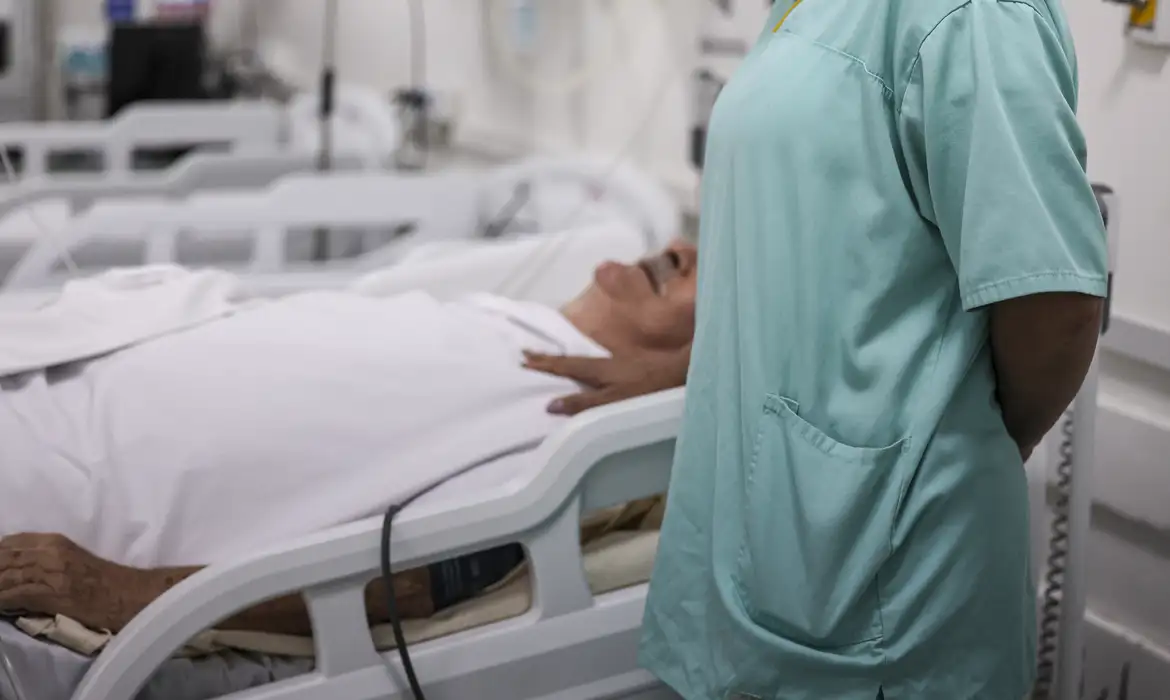
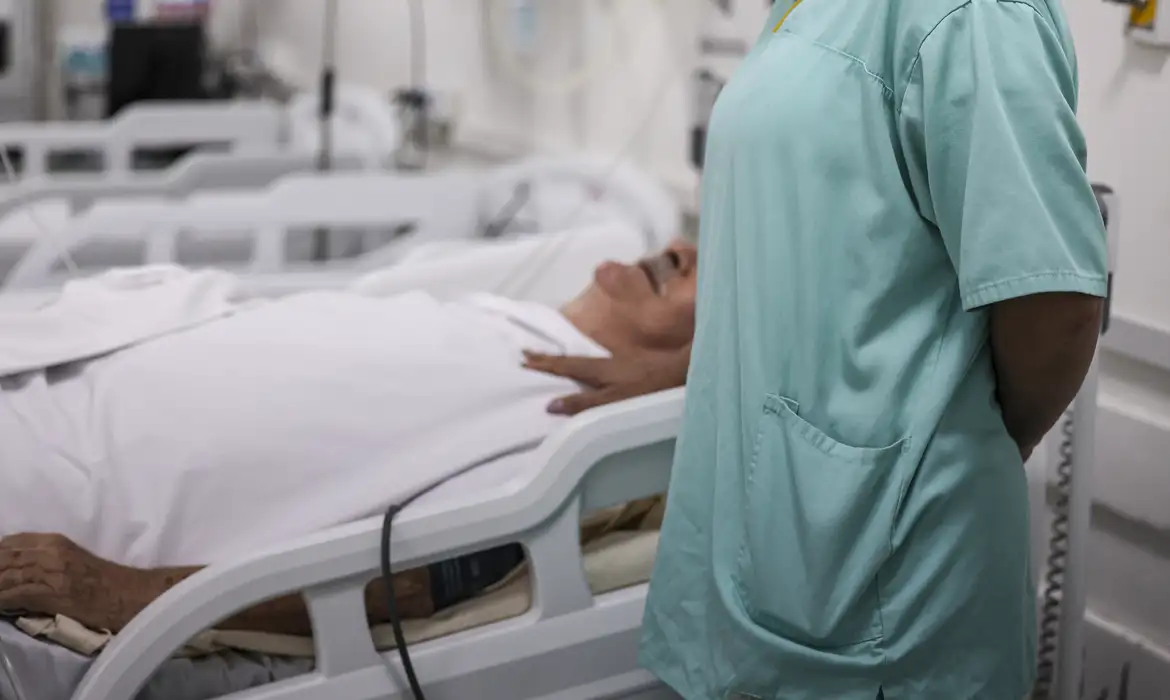
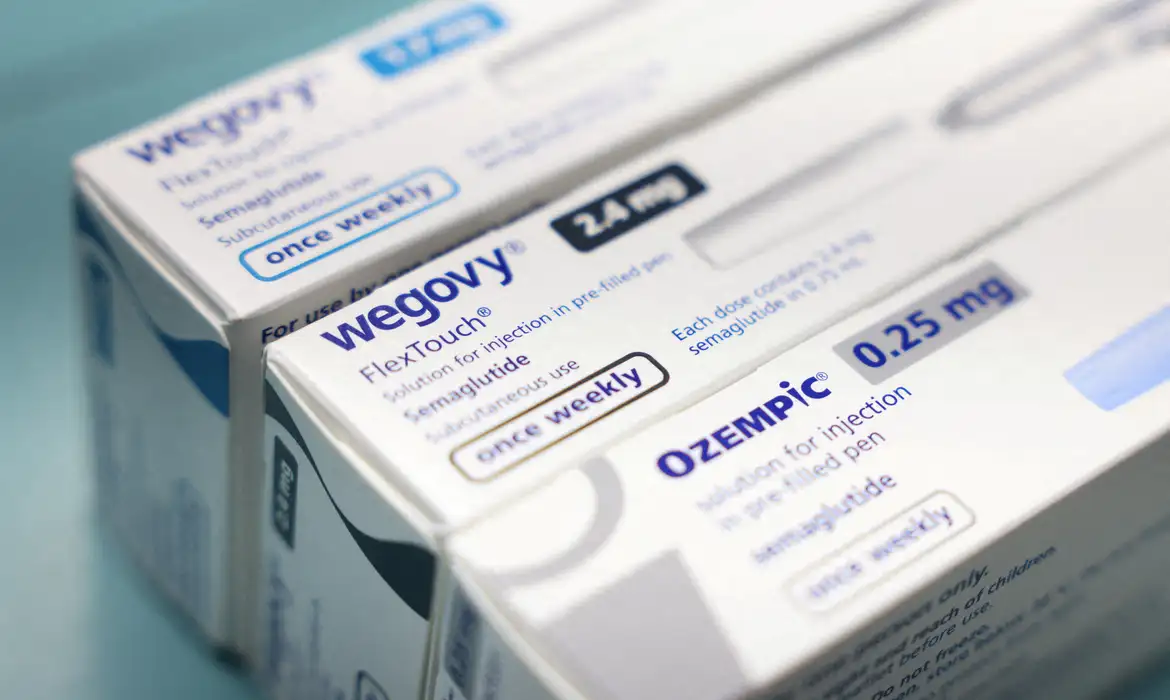
A partir desta sexta-feira, 20 de outubro, a patente da semaglutida no Brasil chega ao fim. Essa substância é o princípio ativo de medicamentos amplamente conhecidos, como o Ozempic, frequentemente chamados de “canetas emagrecedoras”. A expiração da patente significa que novas versões do medicamento, potencialmente mais baratas, poderão ser comercializadas no país.
Atualmente, a Agência Nacional de Vigilância Sanitária (Anvisa) já analisa oito processos para o registro de novos medicamentos com o mesmo princípio ativo. A expectativa é que a concorrência possa democratizar o acesso a esses tratamentos, que têm ganhado popularidade no combate ao diabetes tipo 2 e na perda de peso.
Apesar da boa notícia para os consumidores, a Anvisa ressalta que a aprovação de novas versões da semaglutida, especialmente os chamados análogos sintéticos, apresenta desafios técnicos significativos. O processo de avaliação é rigoroso e visa garantir a segurança e eficácia dos produtos que chegarão ao mercado. Conforme informação divulgada pela Anvisa, o fim da patente da semaglutida abre caminho para análises de novas versões do medicamento.
Anvisa emite parecer sobre novos registros de Semaglutida
A Anvisa informou que dois pedidos de registro de semaglutida sintética estão em fase de exigência, aguardando a apresentação de dados adicionais pelas empresas. Os prazos para resposta das companhias se estendem até o final de junho, o que impossibilita a definição de datas exatas para a conclusão dos processos. Além disso, um produto biológico está em análise e outro aguarda o início da avaliação.
Os demais pedidos em avaliação devem ter um posicionamento das áreas técnicas até o final de abril. Essa posição pode resultar na aprovação, reprovação ou na solicitação de exigências técnicas. A agência reguladora tem dado atenção especial aos análogos sintéticos da semaglutida, considerados um desafio global.
Desafios técnicos na aprovação de análogos sintéticos
Medicamentos registrados atualmente com semaglutida são classificados como produtos biológicos. Os novos pedidos em análise podem ser de dois tipos: biossimilares, obtidos por via biológica, ou sintéticos, produzidos por síntese química. Estes últimos são conhecidos como análogos sintéticos de peptídeos biológicos.
A Anvisa explica que, no caso de medicamentos biológicos, não há a opção de registro como genéricos. Por isso, os produtos devem se enquadrar nas categorias de biossimilares ou análogos sintéticos. Estes últimos exigem uma avaliação criteriosa, combinando parâmetros de fármacos sintéticos e biológicos.
A avaliação de análogos sintéticos de semaglutida é um desafio para agências reguladoras no mundo todo, pois nenhuma das principais agências internacionais, como as do Japão, Europa e Estados Unidos, registrou tais produtos até o momento. A complexidade reside na necessidade de avaliar impurezas, resíduos de solventes, catalisadores metálicos, risco de imunogenicidade e formação de agregados, entre outros aspectos.
Principais pontos de atenção na avaliação pela Anvisa
A Anvisa foca sua atenção técnica em ensaios de impurezas, formação de agregados, garantia de esterilidade e imunogenicidade. O objetivo é assegurar que o medicamento não cause reações imunes indesejadas, como a criação de anticorpos que possam levar à ineficácia do tratamento ou reações mais graves.
A preocupação com a imunogenicidade busca garantir que o medicamento, ao ser administrado, não provoque uma resposta do sistema imunológico do paciente que possa neutralizar seu efeito ou causar efeitos colaterais adversos. Essa análise é crucial para a segurança do paciente.
Decisão judicial sobre a validade das patentes
Em janeiro deste ano, a Quarta Turma do Superior Tribunal de Justiça (STJ) decidiu não admitir a prorrogação das patentes de medicamentos como Ozempic e Rybelsus, que utilizam a semaglutida como princípio ativo. A ação foi movida pela empresa dinamarquesa Novo Nordisk e sua subsidiária brasileira contra o Instituto Nacional da Propriedade Industrial (Inpi).
A disputa judicial buscava o reconhecimento da mora administrativa na tramitação das patentes. No entanto, as instâncias ordinárias negaram os pedidos, baseando-se no entendimento consolidado pelo Supremo Tribunal Federal (STF) de que o prazo de vigência da patente de invenção é de 20 anos a contar do depósito do pedido no Inpi, sendo vedada a sua prorrogação judicial por atrasos administrativos.